FLAVONOID
Flavonoid merupakan sejenis senyawa fenol terbesar yang ada yang memiliki 15 atom karbon, dimana dua cincin benzena yang menyatu dengan rantai karbon tiga linier. Senyawa Flavonoid banyak ditemukan pada tumbuhan dimana senyawa ini memberikan warna pada bunganya. Bagian tanaman yang menghasilkan senyawa Flavnoid ini ialah akar. Warna-warna yang diberikan pada setiap bunga diberikan oleh setiap senyawa Flavonoid itu berbeda-beda, Flavin memberikan warna kuning atau jingga pada bunga, antodianin memberikan warna merah, ungu atau biru (semua warna pelangi kecuali hijau). Selain berperan sebagai pemberi warna, flavonoid juga berperan dalam menentukan rasa, bau dan kualitas nutrisi makanan.
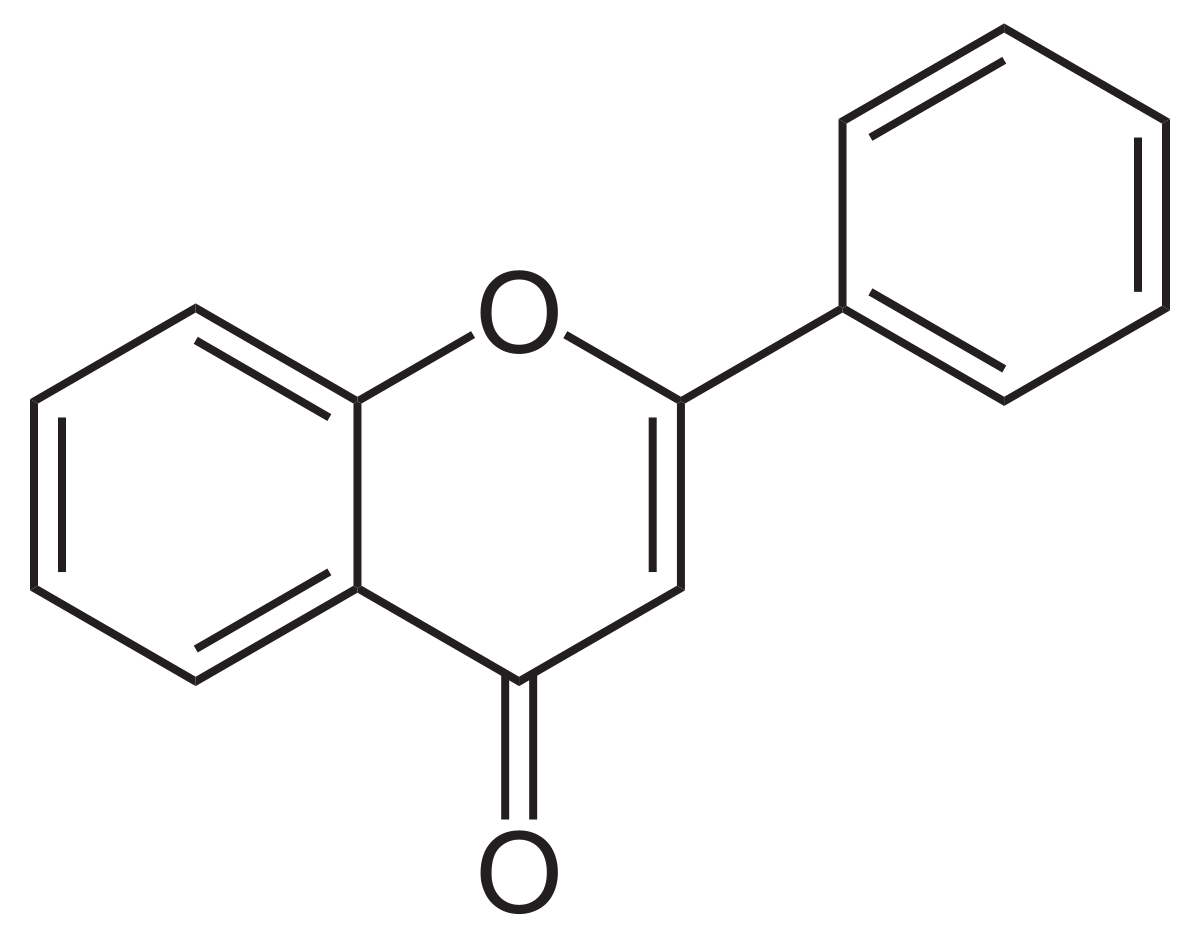
Ciri-ciri struktur flavonoid:
- Cincin A mengalami oksigenasi berselang-seling pada posisi 2,4 dan 6. dan cincin A memeliki gugus hidroksil sehingga memberika kemungkinan terbentuk cincin heterosiklik dalam senyawa trisiklik.
- Cincin B memiliki satu gugus fungsi oksigen pada posisi para atau dua pada posisi para dan meta atau tiga pada di posisi para satu dan di posisi meta dua.

Ciri-ciri struktur flavonoid:
- Cincin A mengalami oksigenasi berselang-seling pada posisi 2,4 dan 6. dan cincin A memeliki gugus hidroksil sehingga memberika kemungkinan terbentuk cincin heterosiklik dalam senyawa trisiklik.
- Cincin B memiliki satu gugus fungsi oksigen pada posisi para atau dua pada posisi para dan meta atau tiga pada di posisi para satu dan di posisi meta dua.
Klasifikasi senyawa flavonoid:
 Flavonoid merupakan metabolit sekunder yang paling beragam dan tersebar luas. Senyawa flavonoid ini sekitar 5-10% metabolit sekunder. Flavonoid banyak ditemukan terutama didalam tumbuhan hijau kecuali alga. Sebenarnya flavonoid ini ditemukan disemua bagian tumbuhan bukan hanya akar seperti batang, daun, bunga, buah, kulit, tepung sari, biji. Sekitar 2% karbon diubah menjadi Flavonoid ketika difotosintesis oleh tumbuhan. Struktur Flavonoid (C6-C3C6) dimana didalamnya terdapat satu cincin teroksigenasi dan dua cincin aromatis. Substitusi gugus kimia Flavonoid umunya melalui hidroksilasi, metoksilasi, metilasi, dan glikosilasi.
Flavonoid merupakan metabolit sekunder yang paling beragam dan tersebar luas. Senyawa flavonoid ini sekitar 5-10% metabolit sekunder. Flavonoid banyak ditemukan terutama didalam tumbuhan hijau kecuali alga. Sebenarnya flavonoid ini ditemukan disemua bagian tumbuhan bukan hanya akar seperti batang, daun, bunga, buah, kulit, tepung sari, biji. Sekitar 2% karbon diubah menjadi Flavonoid ketika difotosintesis oleh tumbuhan. Struktur Flavonoid (C6-C3C6) dimana didalamnya terdapat satu cincin teroksigenasi dan dua cincin aromatis. Substitusi gugus kimia Flavonoid umunya melalui hidroksilasi, metoksilasi, metilasi, dan glikosilasi.
Klasifikasi flavonoid ini sangatlah beragam, diantaranya diklasifikasi menjadi flavon, flavonon, isoflavon, flavanon, antosianin, dan kalkon. Jumlah senyawa flavonoid ini banyak ditemukan dialam, sekitar 6467 sudah diindentifikasi dan jumlah tersebut akan terus meningkat. Bentuk Flavonoid ini beragam yaitu berbentuk monomer, dimer, trimer, tetramer, dan polimer namun bentuk monomer yang paling banyak ditemukan.
Nama senyawa Flavonoid diberikan untuk senyawa fenon yang berasal dari kata flavon (fenol terbesar). Kerangka dari senyawa flavon ini terdiri dari 2-fenilkroman, dimana orto terletak di cincin A dan atom karbon terikat pada cincin B dari 1,3 diarilpropana dihubungkan oleh jembatan oksigen yang akan membentuk cincin heterosiklik yang baru (cincin C).
Dilihat dari tingkat oksidasinya dari rantai propane senyawa flavonoid tebagi menjadi beberapa macam. Jenis senyawa flavonoid yang paling banyak ditemukan dialam yatu Flavon, Falavonon, antosianidin, karena paling banyak ditemukan dialam maka ketiga senyawa tersebut dikatakan flavonoid utama. Senyawa isoflavonida dan neoflavonoida dapat ditemukan pada beberapa jenis tumbuhan terutama suku leguminosae. Masing-masing jenis senyawa flavonoid ini memiliki struktur dasar tertentu.
Flavonoid memiliki kerangka dasar yang terdiri dari 15 atom karbon, dimana terdapat dua cincin benzena (C6) yang terikat pada satu rantai propana (C3) sehingga membentuk suatu susunan (C6-C3-C6). Dengan susunn tersebut maka menghasilkan tiga jenis struktur senyawa flavanoid, diantaranya:
1. Flavonoida ( 1,3-diarilpropana), beberapa senyawa Flavonoida yang ditemukan dialam:
a) Antosianin
Antosianin merupakan pewarna yang paling penting bagi tumbuhan. Antosianin ini turunan dari sianidin. Antosianin tidak dapat larut dalam larutan netral atau basa, sehingga ketika diekstraki digunakan pelarut asam seperti asam asetat dan asam hidroklorida.
Stabiltas antosianin : Stabilitasnya rendah. Jika dalam keadaan panas yag tinggi kestabilan dan ketahanan zat warnanya akan berubah dan bahkan bisa mengakibatkan kerusakan. Selain dengan suhu, pH juga dapat mempengaruhi warnanya, dimana pada suasana asam akan menghasilkan warna merah sedangkan pada suasana basa akan menghasilkan warna biru. Dalam suasana asam Antosianin lebih stabil dibandingkan dalam suasana basa dan netral. Warna pigmen antosianin merah, biru, violet, biasanya dijumpai dalam bunga, buah, dan sayur. Sewaktu pemanasan dalam asam mineral pekat, antosianin pecah menjadi antosianidin dan gula. Pada pH yang rendah pigmennya berwarna merah sedangkan pada pH tinggi pigmenya berwarna violet dan kemudian menjadi biru.
b) Flavonol
Flavonol yang paling alami adalah galagin ( 3,5,7-trihidroksiflavon) dan yang paling rumit adalah hibissetin (3,5,7,8,3',4',5' heptahidroksiflavon). Kebanyakan dari flavonol berbentuk 3-glikosida. Meskipun flavon, flavonol, dan flavanon sama-sama terdistribusi dari tumbuhan tinggi namun tidak ditemukan hubungan khemotakson yang jelas.
c) Khalkon
Khalkon terdapat dialam namun tidak biasa ditemukan terdistribusi di alam, karena khalkon mudah mengalami isomerasi menjadi flavanon dalam satuan kesetimbangan. Cntoh beberapa senyawa kalkon yaitu merein, kereopsin, stillopsin, lanseolin yang umumnya terdapat didalam tanaman. Senyawa khalkon ini umumnya memebrikan pigmen berwarna kuning pada bunga dan paling banyak ditemukan dalam tanaman heliantheaetribe, Coreopsidinae substribe, dan family compositea.
d) Flavon
Dalam keadaan asam flavon stabil dan eternya kan mudah didealkilasi dengan menambahkan HI dan HBr. Selama demetilasi pengaruh asam kuat dapat menyebabkan pembukaan cincin dimana akan membuat tata ulang sering teramati. Contohnya dapat dilhat pada senyawa demetilasi 5,8-dimetoksiflavon dengan penambahan HBr dalam keadaan asam (dalam asam asetat) dimana hal ini menghasilkan 5,6 dihidroksiflavon. Dan pembukaan lanjut dapat terjadi lagi, dimetilasi gugus 5-metoksi dalam polimetoksiflavon yang terjadi pada kondisi/keadaan yang cocok, dengan hal ini akan mudah dibuat 5-hidroksi-polimetoksiflavon.
2. Isoflavonoida (1,2-diarilpropana) : struktur dasarnya terdiri dari C6-C3-C6 dan umunnya dinsintesa oleh tumbuh-tumbuhan dan asam amino. Biosintesanya berlangsung secara bertahap dan memalui beberapa senyawa, seperti asam sinnamat, asam kumarat, calkon, flavon dan isoflavon. Jika dilihat dari biosintesanya maka isoflavon digolongkan kedalam metabolit sekunder, namun didalam mikroba (bakteri, alga, jamur, lumut) tidak mengandung isoflavon meskipun isoflavon tergolong kedalam metaboli sekunder. Hal ini dikarenakan didalam tubuh mikroba tersebut tidak dapat mensintesisnya. Isoflavon banyak ditemukan di alam dan pemanfaatannya juga beragam, berikut pemanfaatannya sebagai obat-obatan/keperluan kesehatan:
a). Anti-inflamasi
Jenis senyawa flavonoid yang dapat berfungsi sebagai anti-inflamasi ini adalah toksifolin, biazilin, haematoksilin, gosipin, prosianidin, nepritin, dll. Dikatakan dapat menjadi anti-inflamasi karena senyawa ini dapat meningkatkan viabilitas sel, dengan hal itu maka jalur metabolisme tidak terhambat.
b). Anti-tumor/Anti-kanker
Senyawa isoflavon yang berpotensi sebagai anti-tumor/anti-kanker ini adalah genistein, genistein ini banyak ditemukan dalam kedelai dan tempe. Mekanisme kerja dari genistein ini sebagai penghambat sel kanker melalui penghambatan pembelahan sel, penghambatan aktivitas enzim DNA isomerase, penghambatan siklus sel, sebagai antioksidan.
c). Anti-virus
Senyawa isoflavon ini dapat menghambat sintesa asam nukleat sehingga menghambat virus berkembang. Seperti yang telah diuji coba pada penyakit demam, hepatitis B.
d). Anti-alergi
Senyawa isoflavon dapat menghambat pembebasan histamin dari sel, senyawa isoflavon yang digunakan sebagai anti-alergi ini ialah terbukronil, proksikromil, dan senyawa kromon.
3. Neoflavonoid (1,1-diarilpropana): senyawa neoflavonoid ini meliputi jenis dari 4-arilkumarin dan dalbergoin.
Flavonoid dapat juga digolongkan berdasarkan jenis ikatannya, antara lain:
a. Flavonoid O-glikosida
Senyawa Flavonoid terikat pada satu gugus gula atau lebih dengan membentuk ikatan hemisetal yang tidak tahan terhadap asam. Dengan adanya glikosida ini maka senyawanya kurang reaktif dan mudah larut dalam air. Biasanya gula yang terikat didalamnya yaitu glukosa, dan juga seperti galaktosa, remilosa, silosa, arabinosa, fruktosa, dan kadang juga glukoronat dan galakturonat. Selain itu disakarida juga dapat terikat, seperti soforosa, gentibiosa, rutinosa dll.
b. Flavonoid C-Glikosida
Gugus gulanya terikat pada inti benzennya dengan suatu ikatan karbon -karbon yang tahan terhadap asam. Biasanya gula tersebut terikat pada atom C yang bernomor 6 dan juga 8. Gula yang biasanya terikat disini ialah galaktosa, raminosa, silosa, arabinosa.
c. Flavonoid sulfat
Senyawa ini mengandung satu atau lebih ion sulfat yang terikat dengan gugus OH fenol atau gula, termasuk juga bisulfate karena terdapat flavon O-SO3K. Yang paling banyak yaitu glikosida bisulfate yang terikat dengan gugus OH fenol atau gula. Umumnya senyawa ini hanya terdapat pada tumbuhan yang mempunyai habitat di air yaitu Angiospermae.
d. Biflavonoid
Senyawa ini awalnya ditemukan dalam ekstrak daun G.biloba yang berwarna kuning dan dinamakan oleh Furukuwa sebagai senyawa ginkgetin (I-4', I-7-tetrahidroksi, II-4'. I-5, II-5, II-7 tetrahidroksi [I-3', II-8] biflavon). Biflavonoid atau nama lainnya biflavonil atau flavandiol merupakan gabungan dua unit flavon atau gabungan dari flavon dengan flavanon dan atau auron. Biflavanoid struktur dasar yaitu 2,3-dihidroapigeninil-(I-3',II-3')-apigenin. Senyawa ini memiliki ikatan interflavanil (C-C) dan terkadang juga terdapat ikatan interflavanil (C-O-C). Senyawa biflavanoid ini banyak ditemukan di alam terutama pada buah, sayur dan bagian tumbuhan lainnya.
Sifat Senyawa Flavanoid :
- senyawanya bersifat asak dikarenakan termasuk kedalam senyawa polifenol
- dapat larut dalam basa
- dapat larut dalam pelarut polar seperti metanol, etanol, aseton, air, butanol, dll karena senyawa ini memiliki gugus hidroksil yang menyebabkannya bersifat polar
- mudah larut dalam air karena pada senyawa ini terdapat gugus glikosida
Jika ditinjau dari sifat kelarutannya flavanoid terbagi menjadi beberapa macam, antara lain:
1. Flavanoid bebas dan aglikon (dalam eter)
2. O-Glikosida (dalam etil asetat)
3. C-Glikosida dan leukoantosianin (dalam butanol dan amil alkohol)
Isolasi dan Identifikasi Flavanoid
1. Isolasi dengan metanol
Isolasi ini dilakukan dua tahap, ekstrak yang sudah dihaluskan tersebut akan dilakukan isolasi dengan metanol:air dengan dua perbandingan yang pertama 9:1 dan yang kedua 1:1, campurannya dibiarkan 6-12 jam. Disaring dan kedua hasil ekstrak tersebut disatukan dan diuapkan hingga 1/3 volume awal atau sampai semua metanol habis.
2. Isolasi dengan Charaux Paris
ekstrak yang digunakan dicampurkan dengan metanol kemudian diuapkan sampai kental, lalu ditambahkan air panas dengan volume yang sama. Lalu ditambahkan eter, dilakukan pemisahan eter dan kemudian diuapkan sampai kering. Hasil dari fase air itu ditambahkan kembali etil. kemudian asetat itu diuapkan yang kemudian didapatkan flavanoid O glikosida
3. Isolasi dengan beberapa pelarut
Disini tidak digunakan ekstrak tetapi menggunakan serbuk kering, serbuknya itu dicampurkan dengan kloroform dan etanol, ektrak etanolnya tersebut kemudian dilarutkan dalam air dan kemudian diekstrak menggunakan dietil eter dan n-butanol, sehingga didapatkan 3 fraksi yaitu fraksi kloroform, butanol dan dietil eter.
4. Identifikasi dengan reaksi warna
a. Uji Wilstrater : warna yang dihasilkan dari reaksi ini ialah
- jingga untuk golongan flavon
- merah krimson untuk golongan flavonol
- merah tua untuk golongan flavonon
b. Uji Bate Smith Matecalve
reaksi ini digunakan untuk mengidentifikasi senyawa leukoantosianin dimana akan dihasilkan warna merah atau ungu jika terkandung senyawa tersebut didalamnya.
Permasalahan:
1. Apakah yang menyebabkan sehingga senyawa Flavonoid ini dapat membantu tumbuhan dalam mempertahankan diri dari serangan penyakit?
2. Jika didalam tumbuhan terdapat dua senyawa flavonoid yang berbeda (misalnya flavin dan antodianin) bagaimanakah pemberian warna untuk bunganya?
3. Flavanoid dikatakan dapat menentukan warna, bau, rasa, serta kualitas nutrisi makanan pada tumbuhan, jadi apakah peran senyawa Flavonoid ini pada hewan?

Klasifikasi flavonoid ini sangatlah beragam, diantaranya diklasifikasi menjadi flavon, flavonon, isoflavon, flavanon, antosianin, dan kalkon. Jumlah senyawa flavonoid ini banyak ditemukan dialam, sekitar 6467 sudah diindentifikasi dan jumlah tersebut akan terus meningkat. Bentuk Flavonoid ini beragam yaitu berbentuk monomer, dimer, trimer, tetramer, dan polimer namun bentuk monomer yang paling banyak ditemukan.
Nama senyawa Flavonoid diberikan untuk senyawa fenon yang berasal dari kata flavon (fenol terbesar). Kerangka dari senyawa flavon ini terdiri dari 2-fenilkroman, dimana orto terletak di cincin A dan atom karbon terikat pada cincin B dari 1,3 diarilpropana dihubungkan oleh jembatan oksigen yang akan membentuk cincin heterosiklik yang baru (cincin C).
Dilihat dari tingkat oksidasinya dari rantai propane senyawa flavonoid tebagi menjadi beberapa macam. Jenis senyawa flavonoid yang paling banyak ditemukan dialam yatu Flavon, Falavonon, antosianidin, karena paling banyak ditemukan dialam maka ketiga senyawa tersebut dikatakan flavonoid utama. Senyawa isoflavonida dan neoflavonoida dapat ditemukan pada beberapa jenis tumbuhan terutama suku leguminosae. Masing-masing jenis senyawa flavonoid ini memiliki struktur dasar tertentu.
Flavonoid memiliki kerangka dasar yang terdiri dari 15 atom karbon, dimana terdapat dua cincin benzena (C6) yang terikat pada satu rantai propana (C3) sehingga membentuk suatu susunan (C6-C3-C6). Dengan susunn tersebut maka menghasilkan tiga jenis struktur senyawa flavanoid, diantaranya:
1. Flavonoida ( 1,3-diarilpropana), beberapa senyawa Flavonoida yang ditemukan dialam:
a) Antosianin
Antosianin merupakan pewarna yang paling penting bagi tumbuhan. Antosianin ini turunan dari sianidin. Antosianin tidak dapat larut dalam larutan netral atau basa, sehingga ketika diekstraki digunakan pelarut asam seperti asam asetat dan asam hidroklorida.
Stabiltas antosianin : Stabilitasnya rendah. Jika dalam keadaan panas yag tinggi kestabilan dan ketahanan zat warnanya akan berubah dan bahkan bisa mengakibatkan kerusakan. Selain dengan suhu, pH juga dapat mempengaruhi warnanya, dimana pada suasana asam akan menghasilkan warna merah sedangkan pada suasana basa akan menghasilkan warna biru. Dalam suasana asam Antosianin lebih stabil dibandingkan dalam suasana basa dan netral. Warna pigmen antosianin merah, biru, violet, biasanya dijumpai dalam bunga, buah, dan sayur. Sewaktu pemanasan dalam asam mineral pekat, antosianin pecah menjadi antosianidin dan gula. Pada pH yang rendah pigmennya berwarna merah sedangkan pada pH tinggi pigmenya berwarna violet dan kemudian menjadi biru.
b) Flavonol
Flavonol yang paling alami adalah galagin ( 3,5,7-trihidroksiflavon) dan yang paling rumit adalah hibissetin (3,5,7,8,3',4',5' heptahidroksiflavon). Kebanyakan dari flavonol berbentuk 3-glikosida. Meskipun flavon, flavonol, dan flavanon sama-sama terdistribusi dari tumbuhan tinggi namun tidak ditemukan hubungan khemotakson yang jelas.
c) Khalkon
Khalkon terdapat dialam namun tidak biasa ditemukan terdistribusi di alam, karena khalkon mudah mengalami isomerasi menjadi flavanon dalam satuan kesetimbangan. Cntoh beberapa senyawa kalkon yaitu merein, kereopsin, stillopsin, lanseolin yang umumnya terdapat didalam tanaman. Senyawa khalkon ini umumnya memebrikan pigmen berwarna kuning pada bunga dan paling banyak ditemukan dalam tanaman heliantheaetribe, Coreopsidinae substribe, dan family compositea.
d) Flavon
Dalam keadaan asam flavon stabil dan eternya kan mudah didealkilasi dengan menambahkan HI dan HBr. Selama demetilasi pengaruh asam kuat dapat menyebabkan pembukaan cincin dimana akan membuat tata ulang sering teramati. Contohnya dapat dilhat pada senyawa demetilasi 5,8-dimetoksiflavon dengan penambahan HBr dalam keadaan asam (dalam asam asetat) dimana hal ini menghasilkan 5,6 dihidroksiflavon. Dan pembukaan lanjut dapat terjadi lagi, dimetilasi gugus 5-metoksi dalam polimetoksiflavon yang terjadi pada kondisi/keadaan yang cocok, dengan hal ini akan mudah dibuat 5-hidroksi-polimetoksiflavon.
2. Isoflavonoida (1,2-diarilpropana) : struktur dasarnya terdiri dari C6-C3-C6 dan umunnya dinsintesa oleh tumbuh-tumbuhan dan asam amino. Biosintesanya berlangsung secara bertahap dan memalui beberapa senyawa, seperti asam sinnamat, asam kumarat, calkon, flavon dan isoflavon. Jika dilihat dari biosintesanya maka isoflavon digolongkan kedalam metabolit sekunder, namun didalam mikroba (bakteri, alga, jamur, lumut) tidak mengandung isoflavon meskipun isoflavon tergolong kedalam metaboli sekunder. Hal ini dikarenakan didalam tubuh mikroba tersebut tidak dapat mensintesisnya. Isoflavon banyak ditemukan di alam dan pemanfaatannya juga beragam, berikut pemanfaatannya sebagai obat-obatan/keperluan kesehatan:
a). Anti-inflamasi
Jenis senyawa flavonoid yang dapat berfungsi sebagai anti-inflamasi ini adalah toksifolin, biazilin, haematoksilin, gosipin, prosianidin, nepritin, dll. Dikatakan dapat menjadi anti-inflamasi karena senyawa ini dapat meningkatkan viabilitas sel, dengan hal itu maka jalur metabolisme tidak terhambat.
b). Anti-tumor/Anti-kanker
Senyawa isoflavon yang berpotensi sebagai anti-tumor/anti-kanker ini adalah genistein, genistein ini banyak ditemukan dalam kedelai dan tempe. Mekanisme kerja dari genistein ini sebagai penghambat sel kanker melalui penghambatan pembelahan sel, penghambatan aktivitas enzim DNA isomerase, penghambatan siklus sel, sebagai antioksidan.
c). Anti-virus
Senyawa isoflavon ini dapat menghambat sintesa asam nukleat sehingga menghambat virus berkembang. Seperti yang telah diuji coba pada penyakit demam, hepatitis B.
d). Anti-alergi
Senyawa isoflavon dapat menghambat pembebasan histamin dari sel, senyawa isoflavon yang digunakan sebagai anti-alergi ini ialah terbukronil, proksikromil, dan senyawa kromon.
3. Neoflavonoid (1,1-diarilpropana): senyawa neoflavonoid ini meliputi jenis dari 4-arilkumarin dan dalbergoin.
Flavonoid dapat juga digolongkan berdasarkan jenis ikatannya, antara lain:
a. Flavonoid O-glikosida
Senyawa Flavonoid terikat pada satu gugus gula atau lebih dengan membentuk ikatan hemisetal yang tidak tahan terhadap asam. Dengan adanya glikosida ini maka senyawanya kurang reaktif dan mudah larut dalam air. Biasanya gula yang terikat didalamnya yaitu glukosa, dan juga seperti galaktosa, remilosa, silosa, arabinosa, fruktosa, dan kadang juga glukoronat dan galakturonat. Selain itu disakarida juga dapat terikat, seperti soforosa, gentibiosa, rutinosa dll.
b. Flavonoid C-Glikosida
Gugus gulanya terikat pada inti benzennya dengan suatu ikatan karbon -karbon yang tahan terhadap asam. Biasanya gula tersebut terikat pada atom C yang bernomor 6 dan juga 8. Gula yang biasanya terikat disini ialah galaktosa, raminosa, silosa, arabinosa.
c. Flavonoid sulfat
Senyawa ini mengandung satu atau lebih ion sulfat yang terikat dengan gugus OH fenol atau gula, termasuk juga bisulfate karena terdapat flavon O-SO3K. Yang paling banyak yaitu glikosida bisulfate yang terikat dengan gugus OH fenol atau gula. Umumnya senyawa ini hanya terdapat pada tumbuhan yang mempunyai habitat di air yaitu Angiospermae.
d. Biflavonoid
Senyawa ini awalnya ditemukan dalam ekstrak daun G.biloba yang berwarna kuning dan dinamakan oleh Furukuwa sebagai senyawa ginkgetin (I-4', I-7-tetrahidroksi, II-4'. I-5, II-5, II-7 tetrahidroksi [I-3', II-8] biflavon). Biflavonoid atau nama lainnya biflavonil atau flavandiol merupakan gabungan dua unit flavon atau gabungan dari flavon dengan flavanon dan atau auron. Biflavanoid struktur dasar yaitu 2,3-dihidroapigeninil-(I-3',II-3')-apigenin. Senyawa ini memiliki ikatan interflavanil (C-C) dan terkadang juga terdapat ikatan interflavanil (C-O-C). Senyawa biflavanoid ini banyak ditemukan di alam terutama pada buah, sayur dan bagian tumbuhan lainnya.
Sifat Senyawa Flavanoid :
- senyawanya bersifat asak dikarenakan termasuk kedalam senyawa polifenol
- dapat larut dalam basa
- dapat larut dalam pelarut polar seperti metanol, etanol, aseton, air, butanol, dll karena senyawa ini memiliki gugus hidroksil yang menyebabkannya bersifat polar
- mudah larut dalam air karena pada senyawa ini terdapat gugus glikosida
Jika ditinjau dari sifat kelarutannya flavanoid terbagi menjadi beberapa macam, antara lain:
1. Flavanoid bebas dan aglikon (dalam eter)
2. O-Glikosida (dalam etil asetat)
3. C-Glikosida dan leukoantosianin (dalam butanol dan amil alkohol)
Isolasi dan Identifikasi Flavanoid
1. Isolasi dengan metanol
Isolasi ini dilakukan dua tahap, ekstrak yang sudah dihaluskan tersebut akan dilakukan isolasi dengan metanol:air dengan dua perbandingan yang pertama 9:1 dan yang kedua 1:1, campurannya dibiarkan 6-12 jam. Disaring dan kedua hasil ekstrak tersebut disatukan dan diuapkan hingga 1/3 volume awal atau sampai semua metanol habis.
2. Isolasi dengan Charaux Paris
ekstrak yang digunakan dicampurkan dengan metanol kemudian diuapkan sampai kental, lalu ditambahkan air panas dengan volume yang sama. Lalu ditambahkan eter, dilakukan pemisahan eter dan kemudian diuapkan sampai kering. Hasil dari fase air itu ditambahkan kembali etil. kemudian asetat itu diuapkan yang kemudian didapatkan flavanoid O glikosida
3. Isolasi dengan beberapa pelarut
Disini tidak digunakan ekstrak tetapi menggunakan serbuk kering, serbuknya itu dicampurkan dengan kloroform dan etanol, ektrak etanolnya tersebut kemudian dilarutkan dalam air dan kemudian diekstrak menggunakan dietil eter dan n-butanol, sehingga didapatkan 3 fraksi yaitu fraksi kloroform, butanol dan dietil eter.
4. Identifikasi dengan reaksi warna
a. Uji Wilstrater : warna yang dihasilkan dari reaksi ini ialah
- jingga untuk golongan flavon
- merah krimson untuk golongan flavonol
- merah tua untuk golongan flavonon
b. Uji Bate Smith Matecalve
reaksi ini digunakan untuk mengidentifikasi senyawa leukoantosianin dimana akan dihasilkan warna merah atau ungu jika terkandung senyawa tersebut didalamnya.
Permasalahan:
1. Apakah yang menyebabkan sehingga senyawa Flavonoid ini dapat membantu tumbuhan dalam mempertahankan diri dari serangan penyakit?
2. Jika didalam tumbuhan terdapat dua senyawa flavonoid yang berbeda (misalnya flavin dan antodianin) bagaimanakah pemberian warna untuk bunganya?
3. Flavanoid dikatakan dapat menentukan warna, bau, rasa, serta kualitas nutrisi makanan pada tumbuhan, jadi apakah peran senyawa Flavonoid ini pada hewan?
Saya Friska Utami (A1C117021) akan menjawab pertanyaan no.1. Menurut saya, penyebab senyawa flavonoid dapat membantu tumbuhan dalam mempertahankan diri adalah karena senyawa flavonoid merupakan senyawa metabolit sekunder. Yang man senyawa metabolit sekunder ini berfungsi sebagai pertahanan diri tumbuhan dari serangan penyakit dan hama.
BalasHapusHallo seprida
BalasHapusSaya akan mencoba menjawab permasalahan yang no.3. menurut saya didalam tubuh hewan juga tersusun senyawa flavonoid. Namun flavonoid didalam tubuh hewan tidak sebanyak didalam tubuh tumbuhan. Didalam hewan flavonoid ini berperan sebagai ekologi hewan itu sendiri.
2. Dari penjelasan sebelumnya bahwa senyawa flavonoid ini dapat memberikan pengaruhnya terhadap keindahan warna pada bunga di alam. Beberapa senyawa flavonoid yang dapat memberikan warnanya pada tumbuhan itu sendiri salah satu contohnya yaitu senyawa flavin yang memberikan warna jingga dan kunig, dan senyawa anthocyanin yang memberikan warna ungu, biru dan merah. Jadi menurut saya tidak masalah jika ada tumbuhan yang memiliki 2 keindahan pada warnanya, salah satu contohnya adalah bunga two tone rose. Dan juga Warna anthocyanin tergantung pada pH.
BalasHapus